বেরিলিয়াম (বি), পূর্বে (১৯৫7 অবধি) গ্লুকিনিয়াম, রাসায়নিক উপাদান, পর্যায় সারণীর গ্রুপ ২ (IIA) এর ক্ষার-পৃথিবী ধাতব হালকা সদস্য, যা শক্তকরণকারী এজেন্ট হিসাবে ধাতববিদ্যায় এবং বহিরাগত স্থান এবং পারমাণবিক প্রয়োগগুলিতে ব্যবহৃত হয় ।
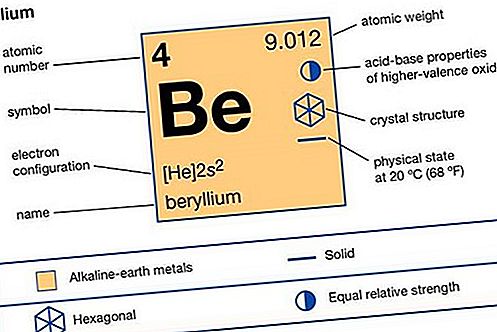

ক্ষার-পৃথিবী ধাতু
উপাদানগুলি হ'ল বেরিলিয়াম (বি), ম্যাগনেসিয়াম (এমজি), ক্যালসিয়াম (সিএ), স্ট্রন্টিয়াম (এসআর), বেরিয়াম (বা), এবং রেডিয়াম (রা)।
উপাদান বৈশিষ্ট্য
| পারমাণবিক সংখ্যা | 4 |
|---|---|
| পারমাণবিক ওজন | 9,0122 |
| গলনাঙ্ক | 1,287 ° C (2,349 ° F) |
| স্ফুটনাঙ্ক | 2,471 ° C (4,480 ° F) |
| আপেক্ষিক গুরুত্ব | 1.85 at 20 ° C (68 ° F) |
| জারণ অবস্থা | +2 |
| ইলেকট্রনের গঠন | 1s 2 2s 2 |
ঘটনা, বৈশিষ্ট্য এবং ব্যবহার
বেরিলিয়াম হ'ল একটি ইস্পাত-ধূসর ধাতু যা ঘরের তাপমাত্রায় বেশ ভঙ্গুর এবং এর রাসায়নিক বৈশিষ্ট্যগুলি কিছুটা অ্যালুমিনিয়ামের সাথে সাদৃশ্যপূর্ণ। প্রকৃতিতে এটি নিখরচায় ঘটে না। বেরিলিয়াম পাওয়া যায় বেরিল এবং পান্না, খনিজগুলি যা প্রাচীন মিশরীয়দের কাছে পরিচিত ছিল known যদিও দীর্ঘদিন ধরেই সন্দেহ করা হয়েছিল যে দুটি খনিজই একই রকম ছিল, 18 তম শতাব্দীর শেষের দিকে এটির রাসায়নিক নিশ্চিতকরণ ঘটেনি। পান্না এখন সবুজ জাতের বেরিল হিসাবে পরিচিত। বেরিলিয়াম (1798) ফরাসী রসায়নবিদ নিকোলাস-লুই ভৌকিলিন অ্যারাইড হিসাবে বেরিল এবং পান্নাতে আবিষ্কার করেছিলেন এবং আলাদাভাবে (1828) ধাতব হিসাবে জার্মান রসায়নবিদ ফ্রিডরিচ ওহলার এবং ফরাসী রসায়নবিদ আন্টোইন এ বি বিসি দ্বারা পটাসিয়ামের ক্লোরাইড হ্রাস করার মাধ্যমে আবিষ্কার করেছিলেন। । বেরিলিয়ামটি পৃথিবীর ভূত্বকগুলিতে ব্যাপকভাবে বিতরণ করা হয় এবং অনুমান করা হয় যে পৃথিবীর আগ্নেয় শিলাগুলিতে 0.0002 শতাংশের সীমাতে ঘটবে। এর মহাজাগতিক প্রাচুর্য 20 স্কেল যেখানে সিলিকন, মান, 1,000,000। মার্কিন যুক্তরাষ্ট্রের বিশ্বের ry০ শতাংশ বেরিলিয়াম রয়েছে এবং এটি এখন পর্যন্ত বেরিলিয়ামের বৃহত্তম উত্পাদনকারী; অন্যান্য প্রধান উত্পাদনকারী দেশগুলির মধ্যে চীন, মোজাম্বিক এবং ব্রাজিল অন্তর্ভুক্ত রয়েছে।
30 সম্পর্কে স্বীকৃত খনিজ পান্না সহ Beryllium, ধারণকারী আছে (আল 2 হউন 3 যদি 6 হে 18, একটি Beryllium অ্যালুমিনিয়াম সিলিকেট), bertrandite (হতে 4 যদি 2 হে 7 (OH) 2, একটি Beryllium সিলিকেট), phenakite (হতে 2 Sio 4), এবং ক্রাইসোবারিল (বিএল 2 ও 4)। (বেরিল, পান্না এবং অ্যাকোয়ামারিনের মূল্যবান রূপগুলি, উপরে বর্ণিত একটি রচনাটি নিকটবর্তী হওয়ার নিকটে রয়েছে, তবে শিল্প আকরিকগুলিতে কম বেরিলিয়াম থাকে; বেশিরভাগ বেরিল অন্যান্য খনন পরিচালনার উপ-পণ্য হিসাবে প্রাপ্ত হয়, বড় স্ফটিকগুলি হাতে নিয়ে যায়) ।) বাণিজ্যিক আকরিক গঠনের জন্য বেরিল এবং বার্ট্রান্ডাইট যথেষ্ট পরিমাণে পাওয়া গেছে যেখান থেকে বেরিলিয়াম হাইড্রক্সাইড বা বেরিলিয়াম অক্সাইড শিল্পজাতভাবে উত্পাদিত হয়। বেরিলিয়ামের নিষ্কাশন এই জটিলতার সাথে জটিল যে, বেশিরভাগ আকরিকগুলিতে বেরিলিয়াম একটি গৌণ উপাদান (খাঁটি বেরিলে ভর দ্বারা 5 শতাংশ, বারট্র্যান্ডাইটে ভর দ্বারা 1 শতাংশেরও কম) এবং অক্সিজেনের সাথে দৃ bound়ভাবে আবদ্ধ থাকে। অ্যাসিডের সাহায্যে চিকিত্সা, জটিল ফ্লোরাইড সহ ভুনা এবং তরল তরল নিষ্কাশন সবই এর হাইড্রোক্সাইড আকারে বেরিলিয়ামকে ঘন করার জন্য নিযুক্ত করা হয়েছে। হাইড্রোক্সাইড অ্যামোনিয়াম বেরিলিয়াম ফ্লোরাইডের মাধ্যমে ফ্লোরাইডে রূপান্তরিত হয় এবং তারপরে ম্যাগনেসিয়াম দিয়ে উত্তপ্ত হয়ে মৌলিক বেরিলিয়াম গঠন করে। বিকল্পভাবে, হাইড্রোক্সাইডকে অক্সাইড গঠনের জন্য উত্তপ্ত করা যেতে পারে, যা কার্বন এবং ক্লোরিনের সাহায্যে চিকিত্সা করে বেরিলিয়াম ক্লোরাইড গঠন করতে পারে; গলিত ক্লোরাইডের তড়িৎ বিশ্লেষণটি তারপরে ধাতব উত্পাদন করতে ব্যবহৃত হয়। উপাদানটি ভ্যাকুয়াম গলানোর মাধ্যমে শুদ্ধ হয়।
অপেক্ষাকৃত উচ্চ গলনাঙ্ক সহ বেরিলিয়াম একমাত্র স্থিতিশীল হালকা ধাতু। যদিও এটি ক্ষার এবং ননঅক্সিডাইজিং অ্যাসিড দ্বারা সহজেই আক্রান্ত হয়, বেরিলিয়াম দ্রুত একটি আনুগত্যকারী অক্সাইড পৃষ্ঠের ফিল্ম গঠন করে যা সাধারণ অবস্থার অধীনে আরও বায়ু জারণ থেকে ধাতুটিকে রক্ষা করে। এই রাসায়নিক বৈশিষ্ট্যগুলি, এর দুর্দান্ত বৈদ্যুতিক পরিবাহিতা, উচ্চ তাপ ক্ষমতা এবং পরিবাহিতা, উচ্চ তাপমাত্রায় ভাল যান্ত্রিক বৈশিষ্ট্য এবং স্থিতিস্থাপকতার খুব উচ্চ মডুলাস (ইস্পাতের চেয়ে এক তৃতীয়াংশ বেশি) কাঠামোগত এবং তাপ প্রয়োগের জন্য এটি মূল্যবান করে তোলে। বেরিলিয়ামের মাত্রিক স্থিতিশীলতা এবং উচ্চ পোলিশ নেওয়ার দক্ষতা স্থান, সামরিক এবং চিকিত্সা অ্যাপ্লিকেশন এবং সেমিকন্ডাক্টর উত্পাদনতে আয়না এবং ক্যামেরা শাটারের জন্য এটি দরকারী করে তুলেছে। অল্প পারমাণবিক ওজন হওয়ায়, বেরিলিয়াম অ্যালুমিনিয়ামের পাশাপাশি 17 বার এক্স-রে সঞ্চারিত করে এবং এক্স-রে টিউবগুলির জন্য উইন্ডো তৈরিতে ব্যাপকভাবে ব্যবহৃত হয়েছে। বেরিলিয়ামটি গাইরোস্কোপ, অ্যাকসিলোমিটার এবং কম্পিউটারের অংশগুলিতে অন্তর্নিহিত নির্দেশিকা যন্ত্র এবং ক্ষেপণাস্ত্র, বিমান এবং মহাকাশ যানবাহনের জন্য অন্যান্য ডিভাইসগুলিতে গড়া হয় এবং এটি ভারী শুল্ক ব্রেক ড্রামস এবং অনুরূপ অ্যাপ্লিকেশনগুলির জন্য ব্যবহৃত হয় যাতে একটি উত্তাপ তাপ ডুবানো গুরুত্বপূর্ণ। এটির দ্রুত নিউট্রনগুলি ধীর করার ক্ষমতা পারমাণবিক চুল্লিগুলিতে যথেষ্ট প্রয়োগ পেয়েছে।
বেশিরভাগ বেরিলিয়াম হ'ল অ্যালয়েগুলির নিম্ন-শতাংশের উপাদান হিসাবে ব্যবহৃত হয়, বিশেষত তামাটি মূল উপাদান হিসাবে তবে নিকেল- এবং লোহা-ভিত্তিক মিশ্রণগুলি যেমন ঝরনার মতো পণ্যের জন্য। বেরিলিয়াম-তামা (2 শতাংশ বেরিলিয়াম) ব্যবহারের জন্য সরঞ্জামগুলিতে তৈরি করা হয় যখন স্পার্কিং বিপজ্জনক হতে পারে, যেমন গুঁড়া কারখানাগুলিতে। বেরিলিয়াম নিজেই স্পার্কিং হ্রাস করে না, তবে এটি তামাটিকে শক্তিশালী করে (6 এর একটি উপাদান দ্বারা), যা প্রভাবের পরে স্পার্কস তৈরি করে না। অক্সিজেনযোগ্য ধাতবগুলিতে অল্প পরিমাণে বেরিলিয়াম যুক্ত হয়ে পৃষ্ঠের ছায়াছবি রক্ষা করে, ম্যাগনেসিয়ামে প্রদাহজনকতা হ্রাস করে এবং রূপোর মিশ্রণগুলিতে কলঙ্কিত হয়।
ব্রিটিশ পদার্থবিদ স্যার জেমস চাদউইক একটি রেডিয়াম উত্স থেকে আলফা কণা দ্বারা বোমা মেরে বেরিলিয়াম থেকে বেরিয়ে আসা কণা হিসাবে নিউট্রনগুলি আবিষ্কার করেছিলেন (1932)। তখন থেকে রেডিয়াম, প্লুটোনিয়াম বা আমেরিকার মতো আলফা ইমিটারের সাথে বেরিলিয়াম মিশ্রিত নিউট্রন উত্স হিসাবে ব্যবহৃত হয়। রেডিয়াম পরমাণুর তেজস্ক্রিয় ক্ষয় দ্বারা প্রকাশিত আলফা কণাগুলি বেরিলিয়ামের পরমাণুগুলির সাথে প্রতিক্রিয়া জানায়, পণ্যগুলির মধ্যে নিউট্রনগুলি বিস্তৃত এনার্জিসহ প্রায় 5 × 10 6 ইলেক্ট্রন ভোল্ট (eV) প্রদান করে। তবে যদি রেডিয়ামকে আবদ্ধ করা হয় তবে আলফা কণাগুলির কোনওটি বেরিলিয়ামে না পৌঁছায়,.০০,০০০ ইভি এর চেয়ে কম শক্তির নিউট্রনগুলি রেডিয়ামের ক্ষয়কারী পণ্যগুলি থেকে আরও অনুপ্রবেশকারী গামা বিকিরণ দ্বারা উত্পাদিত হয়। বেরিলিয়াম / রেডিয়াম নিউট্রন উত্স ব্যবহারের examplesতিহাসিকভাবে গুরুত্বপূর্ণ উদাহরণগুলির মধ্যে রয়েছে জার্মান রসায়নবিদ অটো হান এবং ফ্রেটজ স্ট্রেসমান এবং অস্ট্রিয়ান বংশোদ্ভূত পদার্থবিদ লিস মেইটনার দ্বারা ইউরেনিয়াম বোমাবর্ষণ, যা পারমাণবিক বিচ্ছেদ আবিষ্কার করেছিল (১৯৯৯) এবং ইউরেনিয়ামে উদ্দীপনা সৃষ্টি করেছিল ইতালীয় বংশোদ্ভূত পদার্থবিজ্ঞানী এনরিকো ফার্মি (1942) দ্বারা প্রথম নিয়ন্ত্রিত-ফিশন চেইনের প্রতিক্রিয়া।
একমাত্র প্রাকৃতিকভাবে ঘটে যাওয়া আইসোটোপটি স্থিতিশীল বেরিলিয়াম -9, যদিও অন্য 11 টি সিন্থেটিক আইসোটোপ জানা যায়। তাদের অর্ধ-জীবন 1.5 মিলিয়ন বছর (বেরিলিয়াম -10 এর জন্য, যা বিটা ক্ষয় সহ্য করে) থেকে বেরিলিয়াম -8 (যা দ্বি-প্রোটন নিঃসরণের ফলে ক্ষয় হয়) থেকে 6.7 × 10 −17 সেকেন্ড অবধি রয়েছে । সূর্যের বেরিলিয়াম -7 এর ক্ষয় (53.2-দিনের অর্ধ-জীবন) পর্যবেক্ষণ করা সৌর নিউট্রিনোগুলির উত্স।





![2001: কুব্রিকের একটি স্পেস ওডিসি চলচ্চিত্র [1968] 2001: কুব্রিকের একটি স্পেস ওডিসি চলচ্চিত্র [1968]](https://images.thetopknowledge.com/img/entertainment-pop-culture/5/2001-space-odyssey-film-kubrick-1968.jpg)






