বৈশিষ্ট্যের তুলনা
পর্যায় সারণীর গ্রুপ 16 এর অন্তর্ভুক্ত উপাদানগুলি ইলেক্ট্রন কনফিগারেশন দ্বারা চিহ্নিত করা হয় যেখানে ছয়টি ইলেকট্রন বহিরাগততম শেলটি দখল করে। যেমন একটি বৈদ্যুতিন কাঠামোযুক্ত একটি পরমাণু আরও দুটি যোগ করে আটটি ইলেক্ট্রন একটি স্থিতিশীল শেল গঠন করে, দ্বিগুণ নেতিবাচক চার্জযুক্ত একটি আয়ন উত্পাদন করে। নেতিবাচকভাবে চার্জযুক্ত আয়ন গঠনের এই প্রবণতাটি বৈদ্যুতিনগতিশীলতার বৈশিষ্ট্যগুলিতে (কোভ্যালেন্ট সংমিশ্রণে উপস্থিত থাকলে আংশিক নেতিবাচক চার্জের অনুমান) এবং বৈদ্যুতিন সংযোগ (বৈদ্যুতিন গ্রহণের জন্য একটি নিরপেক্ষ পরমাণুর ক্ষমতা, নেতিবাচক আয়ন গঠন)) এই দুটি বৈশিষ্ট্যই তীব্রতায় হ্রাস পায় কারণ উপাদানগুলি পারমাণবিক সংখ্যায় বৃদ্ধি পায় এবং পর্যায় সারণির 16 কলামের নিচে ভর করে mass অক্সিজেনের মধ্যে ফ্লুরিন ব্যতীত, কোনও উপাদানগুলির সর্বোচ্চ বৈদ্যুতিনগতি এবং বৈদ্যুতিন সংযোগ রয়েছে; এই বৈশিষ্ট্যগুলির মানগুলি তখন গ্রুপের বাকী সদস্যদের তত দ্রুত হ্রাস পায় যেভাবে টেলুরিয়াম এবং পোলোনিয়াম প্রকৃতিতে ধাতব হিসাবে বিবেচিত হয়, যৌগিক গঠনে ইলেক্ট্রন অর্জনের পরিবর্তে হারাতে ঝোঁক।
টেবিলের সমস্ত গ্রুপের মতোই, সবচেয়ে হালকা উপাদান - একটি ক্ষুদ্রতম পারমাণবিক সংখ্যার একটি - এর চরম বা অতিরঞ্জিত বৈশিষ্ট্য রয়েছে। অক্সিজেন, তার পরমাণুর ক্ষুদ্র আকারের কারণে, এর অন্তর্নিহিত শেলের মধ্যে অল্প সংখ্যক ইলেক্ট্রন এবং পারমাণবিক ব্যাসার্ধের তুলনায় নিউক্লিয়াসে প্রচুর প্রোটনগুলির বৈশিষ্ট্য রয়েছে সালফার এবং বাকী চালকোজেনের তুলনায় স্বতন্ত্র বৈশিষ্ট্যযুক্ত। এই উপাদানগুলি যুক্তিসঙ্গতভাবে অনুমানযোগ্য এবং পর্যায়ক্রমিক ফ্যাশনে আচরণ করে।
যদিও পোলোনিয়াম এমপিও টাইপের কয়েকটি বাইনারি যৌগ গঠনে অক্সিডেশন অবস্থা state2 প্রদর্শন করে (যার মধ্যে এম ধাতু) তবে ভারী চ্যালকোজেনগুলি সহজেই নেতিবাচক অবস্থা তৈরি করে না, যেমন +2 এবং +4 এর মতো ইতিবাচক অবস্থার পক্ষে রয়েছে। অক্সিজেন ব্যতীত গ্রুপের সমস্ত উপাদান ইতিবাচক জারণ রাষ্ট্রকে ধরে নিতে পারে, এমনকি এটির মানগুলিও প্রাধান্য পায় তবে সর্বোচ্চ মান, +6 সবচেয়ে ভারী সদস্যদের পক্ষে খুব স্থিতিশীল নয়। যখন এই রাষ্ট্রটি অর্জন করা হয়, তখন পরমাণুর একটি নিম্ন অবস্থায় ফিরে আসার জন্য শক্তিশালী চালিকা শক্তি থাকে, প্রায়শই মৌলিক আকারে। এই প্রবণতাটি এস (VI) যৌগগুলির চেয়ে Se (VI) এবং তে (VI) আরও শক্তিশালী অক্সিডাইজিং এজেন্ট যুক্ত যৌগগুলিকে তৈরি করে। বিপরীতভাবে, সালফাইডস, সেলেনাইডস এবং টেলুরিডস, যার মধ্যে জারণ অবস্থা −2 হয় শক্তিশালী হ্রাসকারী এজেন্টগুলি, সহজেই মুক্ত উপাদানগুলিতে অক্সিডাইজ হয়।
সালফার বা সেলেনিয়াম, এবং অবশ্যই অক্সিজেন নয়, একটি ননমেটাল পরমাণুর জন্য খাঁটি আয়নিক বন্ধন গঠন করে। টেলুরিয়াম এবং পোলোনিয়াম কয়েকটি যৌগ গঠন করে যা কিছুটা আয়নিক হয়; টেলুরিয়াম (চতুর্থ) সালফেট, তে (এসও 4) 2, এবং পোলোনিয়াম (দ্বিতীয়) সালফেট, পিওএসও 4 উদাহরণস্বরূপ ।
গ্রুপ 16 এর আরও একটি বৈশিষ্ট্য যা পর্যায় সারণীর কলামগুলিতে সাধারণত প্রবণতার সাথে সমান্তরালভাবে দেখানো হয় হ'ল কেন্দ্রীয় অণু, এক্স এর আকার হিসাবে সংশ্লেষ এক্স (ওএইচ) এন থাকা অণুগুলির ক্রমবর্ধমান স্থায়িত্ব । কোনও যৌগিক HO ― O ― OH নেই, যেখানে কেন্দ্রীয় অক্সিজেন পরমাণুর একটি ইতিবাচক জারণ অবস্থা থাকবে, এটি এমন একটি শর্ত যা এটি প্রতিরোধ করে। সাদৃশ্যযুক্ত সালফার যৌগটি এইচও ― এস ― ওএইচ, যদিও খাঁটি অবস্থায় জানা যায় না, ধাতব সল্ট, সালফোক্সিলাইটস আকারে কয়েকটি স্থিতিশীল ডেরাইভেটিভ রয়েছে। সালফার, এস (ওএইচ) 4 এবং এস (ওএইচ) 6 এর আরও উচ্চতর হাইড্রোক্স্লেটেড যৌগগুলিও বিদ্যমান নয়, সালফারকে ধনাত্মক জারণ অবস্থার প্রতিরোধের কারণে নয় বরং এস (আইভি) এবং এস এর উচ্চতর চার্জের ঘনত্বের কারণে ঘটায় (VI) বলেছে (পরমাণুর ক্ষুদ্র ব্যাসের তুলনায় প্রচুর পরিমাণে ধনাত্মক চার্জ), যা বৈদ্যুতিন হাইড্রোজেন পরমাণুগুলিকে বিঘ্নিত করে এবং ছাঁটাইয়ের সাথে ছয়টি অক্সিজেন পরমাণুর সমবায় বন্ধনে যোগদানকারী ভিড়, পানির ক্ষতির পক্ষে:
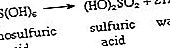
চ্যালকোজেন পরমাণুর আকার বাড়ার সাথে সাথে হাইড্রোক্লিক্লেটেড যৌগগুলির স্থায়িত্ব বৃদ্ধি পায়: যৌগিক অরথোটেলিউরিক অ্যাসিড, তে (ওএইচ) 6, অস্তিত্ব রাখতে সক্ষম।