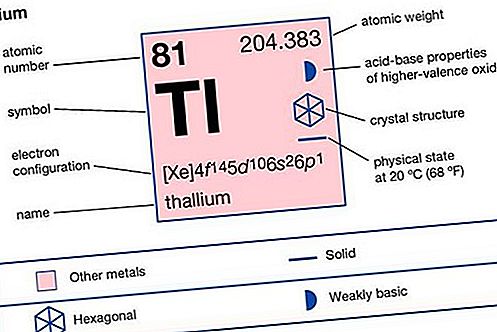
থ্যালিয়াম (টিএল), রাসায়নিক উপাদান, পর্যায় সারণীর প্রধান গ্রুপ ১৩ (IIIa, বা বোরন গ্রুপ) এর ধাতু, বিষাক্ত এবং সীমিত বাণিজ্যিক মূল্য। সীসার মতো, থ্যালিয়াম হ'ল নমনীয় শক্তির নরম, কম গলানোর উপাদান। টাটকা কাটা থ্যালিয়ামে একটি ধাতব ঝলক রয়েছে যা বাতাসের সংস্পর্শে এসে ধূসর বর্ণকে কমিয়ে দেয়। ধাতুটি একটি ভারী অরক্ষিত অক্সাইড ক্রাস্ট তৈরি করে বাতাসের সাথে দীর্ঘায়িত যোগাযোগের পরে জারণ তৈরি করতে থাকে। থ্যালিয়াম হাইড্রোক্লোরিক অ্যাসিডে ধীরে ধীরে দ্রবীভূত হয় এবং সালফিউরিক অ্যাসিড মিশ্রিত করে এবং দ্রুত নাইট্রিক অ্যাসিডে দ্রবীভূত হয়।

বোরন গ্রুপ উপাদান
(গা), ইন্ডিয়াম (ইন), থ্যালিয়াম (টিএল), এবং নিহোনিয়াম (এনএইচ)। বাহ্যিকতম অংশগুলিতে তিনটি ইলেকট্রন রেখে এগুলি একটি গোষ্ঠী হিসাবে চিহ্নিত হয়
।
টিনের চেয়ে বিরল, থ্যালিয়াম কেবলমাত্র কয়েকটি খনিজগুলিতে কেন্দ্রীভূত হয় যার বাণিজ্যিক মূল্য নেই। জাল এবং সীসা এর সালফাইড আকরিকগুলিতে থ্যালিয়ামের পরিমাণ চিহ্নিত করে; এই আকরিকগুলি ভাজায়ে, থ্যালিয়াম ফ্লু ডাস্টগুলিতে ঘন হয়ে যায়, যা থেকে এটি পুনরুদ্ধার হয়।
ব্রিটিশ রসায়নবিদ স্যার উইলিয়াম ক্রুকস সালফিউরিক অ্যাসিড তৈরিতে ব্যবহৃত সেলেনিয়াম-বেয়ারিং পাইরেটস দ্বারা উত্পাদিত বিশিষ্ট সবুজ বর্ণালী রেখার পর্যবেক্ষণ করে (1861) থ্যালিয়াম আবিষ্কার করেছিলেন। ক্রুকস এবং ফরাসি রসায়নবিদ ক্লাউড-অগাস্টে ল্যামি স্বাধীনভাবে বিচ্ছিন্ন (১৮62২) থ্যালিয়ামকে এটিকে ধাতব হিসাবে দেখায়।
উপাদানটির দুটি স্ফটিক রূপগুলি জানা যায়: প্রায় 230 ডিগ্রি সেন্টিগ্রেড (450 ° ফাঃ) এর নীচে নিকট-প্যাকড ষড়ভুজ এবং উপরে দেহকেন্দ্রিক ঘন ঘন। প্রাকৃতিক থ্যালিয়াম, বোরন গ্রুপ উপাদানগুলির মধ্যে সবচেয়ে ভারী, দুটি স্থিতিশীল আইসোটোপের মিশ্রণটি প্রায় সম্পূর্ণভাবে গঠিত: থ্যালিয়াম -203 (29.5 শতাংশ) এবং থ্যালিয়াম -205 (70.5 শতাংশ)। তিনটি প্রাকৃতিক তেজস্ক্রিয় বিভাজন সিরিজের ক্ষয়প্রাপ্ত পণ্য হিসাবে কয়েকটি স্বল্প-স্থায়ী আইসোটোপের চিহ্ন পাওয়া যায়: থ্যালিয়াম -206 এবং থ্যালিয়াম -210 (ইউরেনিয়াম সিরিজ), থ্যালিয়াম -208 (থোরিয়াম সিরিজ), এবং থ্যালিয়াম -207 (অ্যাক্টেনিয়াম সিরিজ)।
থ্যালিয়াম ধাতবটির বাণিজ্যিক ব্যবহার নেই, এবং থ্যালিয়াম যৌগগুলির কোনও বড় বাণিজ্যিক প্রয়োগ নেই, কারণ থ্যালাস সালফেট ১৯ large০ এর দশকে রডেন্টাইসাইড এবং কীটনাশক হিসাবে প্রতিস্থাপন করা হয়েছিল। থ্যালাস যৌগগুলির কয়েকটি সীমিত ব্যবহার রয়েছে। উদাহরণস্বরূপ, ইনফ্রারেড লাইট সংক্রমণকারী মিশ্রিত ব্রোমাইড-আয়োডাইড স্ফটিকগুলি (টিএলবিআর এবং টিএলআই) ইনফ্রারেড অপটিক্যাল সিস্টেমগুলির জন্য লেন্স, উইন্ডো এবং প্রিজমে গড়া হয়েছে। সালফাইড (টিএল 2 এস) একটি ইনফ্রারেড-সংবেদনশীল ফটোসেলে (থ্যালোফাইড সেল) একটি অতি সংবেদনশীল ফটোয়েলেকট্রিক কোষে অক্সিজুলফাইড এবং প্রয়োজনীয় উপাদান হিসাবে নিযুক্ত করা হয়েছে। থ্যালিয়াম তার অক্সাইডগুলিকে দুটি পৃথক জারণ স্থিতি তৈরি করে, +1 (টিএল 2 ও) এবং +3 (টিএল 2 ও 3)। টিএল 2 হে উচ্চতর প্রতিরোধী অপটিকাল চশমাগুলির উপাদান এবং কৃত্রিম রত্নগুলিতে রঙিন এজেন্ট হিসাবে ব্যবহৃত হয়েছে; টিএল 2 ও 3 একটি এন-টাইপ অর্ধপরিবাহী। রেডিয়েশন সনাক্তকরণের জন্য সিন্টিলিলেশন কাউন্টারগুলিতে ব্যবহারের জন্য অজৌবিক ফসফোর তৈরি করতে থ্যালিয়াম যৌগগুলি দ্বারা সোডিয়াম আয়োডাইডের মতো ক্ষারীয় হ্যালাইড স্ফটিকগুলি ডোপড বা সক্রিয় করা হয়েছে।
থ্যালিয়াম একটি বনসান শিখায় একটি উজ্জ্বল সবুজ রঙ সরবরাহ করে। থ্যালাস ক্রোম্যাট, সূত্র টিএল 2 ক্রো 4, থ্যালিয়ামের পরিমাণগত বিশ্লেষণে সবচেয়ে ভাল ব্যবহৃত হয়, যে কোনও থ্যালিক আয়ন, টিএল 3+ এর পরে, নমুনায় উপস্থিত থ্যালাস অবস্থায়, টিএল + এ কমিয়ে দেওয়া হয়েছে ।
থ্যালিঅ্যাম্ একটি গুলি থাকার গ্রুপ 13 উপাদানের আদর্শ 2 পি 1 বাইরের ইলেক্ট্রন কনফিগারেশন। একটি এস থেকে এপ অরবিটালে একটি ইলেকট্রন প্রচার করলে উপাদানটি তিন বা চারটি সমবায় হতে পারে। থ্যালিয়াম সহ, তবে, এস → পি পদোন্নতির জন্য প্রয়োজনীয় শক্তি টিএলএক্স 3 গঠনে পুনরায় ফিরে পাওয়া টিএল এক্স এক্স কোভ্যালেন্ট বন্ড শক্তির তুলনায় উচ্চতর; অতএব, একটি +3 জারণ স্থলযুক্ত একটি ডেরাইভেটিভ খুব জোরালোভাবে অনুকূল প্রতিক্রিয়া পণ্য নয়। সুতরাং, অন্যান্য বোরন গ্রুপ উপাদানগুলির তুলনায় থ্যালিয়াম মূলত +3 জারণ অবস্থার পরিবর্তে +1 তে থ্যালিয়ামযুক্ত এককভাবে চার্জযুক্ত থ্যালিয়াম লবণ তৈরি করে (6s 2 ইলেক্ট্রন অব্যবহৃত থাকে)। বাহ্যিক ইলেক্ট্রন কনফিগারেশন (এন-1) ডি 10 এনএস 2 দিয়ে স্থিতিশীল একা চার্জড কেশন গঠনের একমাত্র উপাদান এটি অসাধারণভাবে যথেষ্ট, জড় গ্যাস কনফিগারেশন নয়। জলে বর্ণহীন, আরও স্থিতিশীল কলুষিত আয়ন, টিএল + ভারী ক্ষারীয় ধাতু আয়ন এবং রৌপ্য সাদৃশ্যযুক্ত; তার +3 অবস্থায় থ্যালিয়ামের যৌগগুলি সহজেই তার +1 অবস্থায় ধাতব সংশ্লেষে কমে যায়।
এর অক্সাইডেশন +3 অবস্থানে, থ্যালিয়াম অ্যালুমিনিয়ামের সাথে সাদৃশ্যযুক্ত, যদিও আয়ন টিএল 3+ খুব বড় আকারের বলেই অঙ্গুলি তৈরি করে। এককভাবে চার্জ করা থ্যালিয়াম আয়ন, টিএল + এবং রুবিডিয়াম আয়ন, আরবি + এর আকারের খুব কাছাকাছি মিল অনেকগুলি টিএল + লবণের তৈরি করে, যেমন ক্রোমেট, সালফেট, নাইট্রেট এবং হালিডস, আইসোমর্ফাস (যেমন, একটি অভিন্ন স্ফটিক রয়েছে) কাঠামো) সম্পর্কিত রুবিডিয়াম লবণের সাথে; এছাড়াও, আয়ন টিএল + আ্যালামগুলিতে আয়ন আরবি + প্রতিস্থাপন করতে সক্ষম । সুতরাং, থ্যালিয়াম একটি পিঠে তৈরি করে, তবে এটি করে এটি এম + আয়নটির পরিবর্তে, এম + এম 3+ (এসও 4) 2 ∙ 12 এইচ 2 ও-তে প্রত্যাশিত ধাতব পরমাণু এম 3+ এর পরিবর্তে ces
দ্রবণীয় থ্যালিয়াম যৌগগুলি বিষাক্ত। আর্দ্র বাতাস বা ত্বকের সংস্পর্শে ধাতু নিজেই এ জাতীয় যৌগগুলিতে পরিবর্তিত হয়। থ্যালিয়াম বিষ, যা মারাত্মক হতে পারে, নার্ভাস এবং গ্যাস্ট্রোইনটেস্টাইনাল ডিসঅর্ডার এবং চুলের দ্রুত ক্ষয় ঘটায়।
উপাদান বৈশিষ্ট্য
| পারমাণবিক সংখ্যা | 81 |
|---|---|
| পারমাণবিক ওজন | 204,37 |
| গলনাঙ্ক | 303.5 ° C (578.3 ° F) |
| স্ফুটনাঙ্ক | 1,457 ° C (2,655 ° F) |
| আপেক্ষিক গুরুত্ব | ১১.৮৮ (২০ ডিগ্রি সেন্টিগ্রেডে [°৮ ডিগ্রি ফারেনহাইট]) |
| জারণ রাষ্ট্র | +1, +3 |
| বৈদ্যুতিন কনফিগার। | [এক্সে] 4 এফ 14 5 ডি 10 6 এস 2 6 পি 1 |



![মুলিগানের একটি মকিংবার্ড চলচ্চিত্রকে হত্যা করার জন্য [1962] মুলিগানের একটি মকিংবার্ড চলচ্চিত্রকে হত্যা করার জন্য [1962]](https://images.thetopknowledge.com/img/entertainment-pop-culture/6/kill-mockingbird-film-mulligan-1962.jpg)