জিরকনিয়াম (জেডআর ), রাসায়নিক উপাদান, পর্যায় সারণীর গ্রুপ 4 (আইভিবি) এর ধাতু, পারমাণবিক চুল্লিগুলির জন্য কাঠামোগত উপাদান হিসাবে ব্যবহৃত হয়।
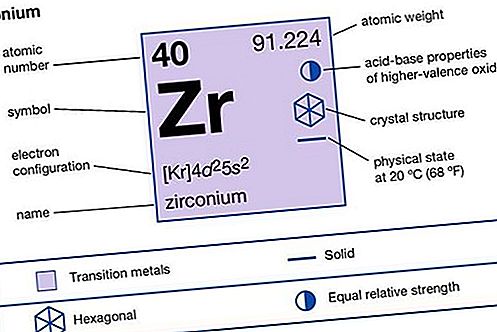
উপাদান বৈশিষ্ট্য
| পারমাণবিক সংখ্যা | 40 |
|---|---|
| পারমাণবিক ওজন | 91,22 |
| গলনাঙ্ক | 1,852 ° C (3,366 ° F) |
| স্ফুটনাঙ্ক | 3,578 ° C (6,472 ° F) |
| আপেক্ষিক গুরুত্ব | 6.49 এ 20 ডিগ্রি সেন্টিগ্রেড (68 ডিগ্রি ফারেনহাইট) |
| জারণ অবস্থা | +4 |
| ইলেকট্রনের গঠন | [কেআর] 4 ডি 2 5 এস 2 |
বৈশিষ্ট্য, উপস্থিতি এবং ব্যবহার
জিরকনিয়াম, 1940 এর দশকের শেষের দিকে অস্পষ্ট, পারমাণবিক শক্তি প্রয়োগের জন্য একটি গুরুত্বপূর্ণ ইঞ্জিনিয়ারিং উপাদান হিসাবে পরিণত হয়েছিল কারণ এটি নিউট্রনের প্রতি অত্যন্ত স্বচ্ছ। জার্মান রসায়নবিদ মার্টিন হেইনিরিক ক্লাপ্রোথ তার অক্সাইড থেকে জিরকন, জিরসিও 4 (জিরকোনিয়াম অরথোসিলিকেট) এ উপাদানটি চিহ্নিত করেছিলেন এবং সুইডিশ রসায়নবিদ জেনস জ্যাকব বার্জিলিয়াসের দ্বারা ধাতুটি অশুচি আকারে বিচ্ছিন্ন করা হয়েছিল (1824)। অপরিষ্কার ধাতু, এমনকি যখন 99 শতাংশ খাঁটি, শক্ত এবং ভঙ্গুর। উচ্চতর বিশুদ্ধতার সাদা, নরম, মলিনযোগ্য এবং নমনীয় ধাতুটি প্রথমে পরিমাণে (1925) উত্পাদিত হয়েছিল ডাচ রসায়নবিদ আন্তন ই ভ্যান আরকেল এবং জেএইচ ডি বোয়ারের জিরকনিয়াম টেট্রায়োডাইডের তাপীয় পচন দ্বারা, জ্রিআরআই 4। 1940 এর দশকের গোড়ার দিকে, লাক্সেমবার্গের উইলিয়াম জাস্টিন ক্রল ম্যাগনেসিয়াম দ্বারা জিরকোনিয়াম টেট্রাক্লোরাইড, জেডক্রিল 4 হ্রাসের উপর ভিত্তি করে ধাতু তৈরির সস্তার প্রক্রিয়াটি বিকাশ করেছিলেন । একবিংশ শতাব্দীর গোড়ার দিকে, জিরকনিয়ামের শীর্ষস্থানীয় উত্পাদকদের মধ্যে অস্ট্রেলিয়া, দক্ষিণ আফ্রিকা, চীন এবং ইন্দোনেশিয়া অন্তর্ভুক্ত ছিল; মোজাম্বিক, ভারত এবং শ্রীলঙ্কা অতিরিক্ত উত্পাদক ছিল।

জিরকোনিয়াম পৃথিবীর ভূত্বকগুলিতে তুলনামূলকভাবে প্রচুর পরিমাণে, তবে ঘন জমাতে নয়, এবং এস-টাইপের তারকাদের মধ্যে বৈশিষ্ট্যযুক্তভাবে পর্যবেক্ষণ করা হয়। খনিজ জিরকন, যা সাধারণত স্ট্রিম বিছানা, সমুদ্র সৈকত বা পুরাতন হ্রদ শয্যাগুলিতে পলল জমার মধ্যে পাওয়া যায়, এটি জিরকনিয়ামের একমাত্র বাণিজ্যিক উত্স। ব্যাডলেইট, যা মূলত খাঁটি জিরকোনিয়াম ডাই অক্সাইড, জেডআরও 2, এটি অন্যান্য গুরুত্বপূর্ণ জিরকোনিয়াম খনিজ, তবে বাণিজ্যিক পণ্যটি জিরকন থেকে আরও সস্তার সাথে পুনরুদ্ধার করা হয়। জিরকনিয়াম একই প্রক্রিয়া দ্বারা উত্পাদিত হয় যেমন টাইটানিয়ামের জন্য ব্যবহৃত হয়। এই জিরকোনিয়াম খনিজগুলিতে সাধারণত একটি হাফনিয়াম সামগ্রী থাকে যা 1 শতাংশের কয়েক দশম থেকে কয়েক শতাংশ পর্যন্ত পরিবর্তিত হয়। কিছু উদ্দেশ্যে দুটি উপাদানের বিভাজন গুরুত্বপূর্ণ নয়: প্রায় 1 শতাংশ হাফনিয়ামযুক্ত জিরকোনিয়াম খাঁটি জিরকোনিয়াম হিসাবে গ্রহণযোগ্য acceptable
জিরকোনিয়ামের সর্বাধিক গুরুত্বপূর্ণ ব্যবহার হ'ল জ্বালানী রডগুলি ক্ল্যাডিংয়ের জন্য, ইউরেনিয়ামের সাথে মিশ্রণ করার জন্য, এবং বৈশিষ্ট্যগুলির অনন্য সংমিশ্রণের কারণে চুল্লি-কোর কাঠামোগুলির জন্য পারমাণবিক চুল্লিগুলিতে। জিরকোনিয়াম উচ্চতর তাপমাত্রায় ভাল শক্তি রাখে, দ্রুত সঞ্চালিত কুল্যান্টগুলি থেকে ক্ষয় প্রতিরোধ করে, উচ্চ তেজস্ক্রিয় আইসোটোপ তৈরি করে না এবং নিউট্রন বোমাবর্ষণ থেকে যান্ত্রিক ক্ষতির বিরুদ্ধে প্রতিরোধ করে। হাফনিয়াম, সমস্ত জিরকোনিয়াম আকরিকগুলিতে উপস্থিত রয়েছে, চুল্লিগুলি ব্যবহারের উদ্দেশ্যে তৈরি ধাতু থেকে অবশ্যই বিস্মৃতভাবে অপসারণ করতে হবে কারণ হাফনিয়াম দৃ neut়ভাবে তাপ নিউট্রন শোষণ করে।
হাফনিয়াম এবং জিরকোনিয়াম পৃথককরণ সাধারণত তরল তরল কাউন্টারকন্ট্র্যান্ট-এক্সট্রাকশন পদ্ধতি দ্বারা সম্পন্ন হয়। পদ্ধতিতে, অশোধিত জিরকোনিয়াম টেট্রাক্লোরাইড অ্যামোনিয়াম থাইওসায়ানেটের জলীয় দ্রবণে দ্রবীভূত হয় এবং মিথাইল আইসোবোটিল কেটোন জলীয় মিশ্রণের সাথে পাল্টে যায়, ফলস্বরূপ যে হাফনিয়াম টেট্রাক্লোরাইড পছন্দসইভাবে উত্তোলিত হয়।
জিরকোনিয়াম এবং হাফনিয়ামের পারমাণবিক রেডিয়ি যথাক্রমে 1.45 এবং 1.44 are হয়, যখন আয়নগুলির রেডিয়ি Zr 4+, 0.74 Å, এবং এইচএফ 4+, 0.75 Å হয় Å পারমাণবিক এবং আয়নিক মাপের ভার্চুয়াল পরিচয়, ল্যান্থানয়েড সংকোচনের ফলে, এই দুটি উপাদানগুলির রাসায়নিক আচরণকে অন্য যে কোনও উপাদান যুক্ত উপাদানগুলির চেয়ে বেশি সাদৃশ্য তৈরি করার প্রভাব ফেলেছে। যদিও হাফনিয়ামের রসায়নটি জিরকিনিয়ামের চেয়ে কম অধ্যয়ন করা হয়েছে, তবে দুটি এতই মিল যে কেবল খুব সামান্য পরিমাণগত পার্থক্য - উদাহরণস্বরূপ, দ্রবণীয়তা এবং যৌগিকগুলির অস্থিরতার ক্ষেত্রে cases এমন ক্ষেত্রে প্রত্যাশিত যেগুলি বাস্তবে তদন্ত করা হয়নি।
জিরকোনিয়াম আশ্চর্যজনক পরিমাণে অক্সিজেন, নাইট্রোজেন এবং হাইড্রোজেন শোষণ করে। প্রায় 800 ° সে (1,500 ডিগ্রি ফারেনহাইট) এটা অক্সিজেনের সঙ্গে রাসায়নিকভাবে সম্মিলন অক্সাইড, ZrO উত্পাদ 2 । জিরকনিয়াম ম্যাগনেসিয়াম, বেরিলিয়াম এবং থোরিয়ামের অক্সাইডগুলির মতো অবাধ্য ক্রুশিবদ্ধ উপকরণকে হ্রাস করে। অক্সিজেন এবং অন্যান্য গ্যাসের জন্য এই দৃ aff় স্নেহ ইলেক্ট্রন টিউবগুলিতে অবশিষ্ট গ্যাসগুলি অপসারণের জন্য প্রাপ্ত হিসাবে ব্যবহার করে। বাতাসের স্বাভাবিক তাপমাত্রায় জিরকনিয়াম অক্সাইড বা নাইট্রাইডের একটি প্রতিরক্ষামূলক ফিল্ম গঠনের কারণে প্যাসিভ হয়। এমনকি এই ফিল্মটি ছাড়াই ধাতব দুর্বল অ্যাসিড এবং অ্যাসিডীয় লবণের ক্রিয়া প্রতিরোধী to এটি হাইড্রোফ্লোরিক অ্যাসিডে সবচেয়ে ভাল দ্রবীভূত হয়, যার পদ্ধতিতে সমাধানটি স্থিতিশীল করার জন্য অ্যানিয়োনিক ফ্লুরো কমপ্লেক্সগুলি গঠন গুরুত্বপূর্ণ। সাধারণ তাপমাত্রায় এটি বিশেষভাবে প্রতিক্রিয়াশীল নয় তবে উন্নত তাপমাত্রায় ননমেটালগুলি দিয়ে বেশ প্রতিক্রিয়াশীল হয়ে ওঠে। উচ্চ জারা প্রতিরোধের কারণে, জিরকনিয়াম পাম্প, ভালভ এবং হিট এক্সচেঞ্জারগুলির বানোয়াটে ব্যাপক ব্যবহার খুঁজে পেয়েছে। জিরকনিয়াম কিছু ম্যাগনেসিয়াম মিশ্রণগুলির উত্পাদনে এবং একটি নির্দিষ্ট স্টিল তৈরিতে একটি সংযোজনকারী হিসাবে এজেন্ট হিসাবে ব্যবহৃত হয়।
প্রাকৃতিক জিরকোনিয়ামটি পাঁচটি স্থিতিশীল আইসোটোপের মিশ্রণ: জিরকোনিয়াম -৯০ (৫১.66 শতাংশ), জিরকোনিয়াম -১৯ (১১.২৩ শতাংশ), জিরকনিয়াম -২২ (১.1.১১ শতাংশ), জিরকিনিয়াম -৪৪ (১..৪০ শতাংশ), জিরকোনিয়াম -৯৯ (২.৮০ শতাংশ)। দুটি অ্যালোট্রপ বিদ্যমান: 862 ডিগ্রি সেন্টিগ্রেডের নিচে (1,584 ° F) একটি ষড়ভুজ ঘনিষ্ঠ-কাঠামোযুক্ত কাঠামো, সেই তাপমাত্রার উপরে দেহকেন্দ্রিক ঘনকূপ।







![কোভাদোঙ্গার যুদ্ধ স্প্যানিশ ইতিহাস [সি। 720] কোভাদোঙ্গার যুদ্ধ স্প্যানিশ ইতিহাস [সি। 720]](https://images.thetopknowledge.com/img/world-history/5/battle-covadonga-spanish-history-c-720.jpg)