বোর্ন, বোরন এবং হাইড্রোজেন বা তাদের ডেরাইভেটিভগুলির অজৈব যৌগগুলির কোনও হোমোলজাস সিরিজের।
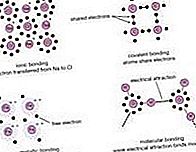
রাসায়নিক বন্ধন: Boranes
ইলেক্ট্রন-ঘাটতি যৌগিক ডাইবোরেন, বি 2 এইচ 6, যেমনটি পূর্বে উল্লিখিত হয়েছিল, একসাথে অনুষ্ঠিত পরমাণুর গুচ্ছ হিসাবে বিবেচিত হতে পারে
।
বোরন হাইড্রাইডগুলি প্রথমে নিয়মিতভাবে সংশ্লেষিত হয়েছিল এবং ১৯১২ সাল থেকে প্রায় 1937 সাল পর্যন্ত জার্মান রসায়নবিদ আলফ্রেড স্টক দ্বারা চিহ্নিত করা হয়েছিল। তিনি তাদের পর্যায় সারণীতে বোরনের প্রতিবেশী কার্বন (সি) এর হাইড্রাইড, অ্যালকানেস (স্যাচুরেটেড হাইড্রোকার্বন) এর সাথে সাদৃশ্য হিসাবে তাদের বোরাণ বলেছিলেন। যেহেতু লাইটার বোর্নগুলি উদ্বায়ী, বায়ু এবং আর্দ্রতার সংবেদনশীল এবং বিষাক্ত ছিল তাই স্টক সেগুলি অধ্যয়নের জন্য উচ্চ শূন্যস্থান পদ্ধতি এবং যন্ত্রপাতি তৈরি করেছিল। বোর্নেস সম্পর্কিত আমেরিকান কাজ 1931 সালে শুরু হয়েছিল, এটি হারম্যান আই শ্লেসিংগার এবং অ্যানটন বি বার্গ দ্বারা পরিচালিত হয়েছিল। আমেরিকা সরকার আইসোটোপ পৃথকীকরণের জন্য উদ্বায়ী ইউরেনিয়াম যৌগগুলি (বোরিহাইড্রাইড) এবং ১৯৫০ এর দশকে গবেষণাকে সমর্থন করেছিল যখন রকেট এবং জেট বিমানের জন্য উচ্চ-জ্বালানী জ্বালানি তৈরির কর্মসূচিকে সমর্থন করেছিল যখন বোরাণরা মূলত দ্বিতীয় বিশ্বযুদ্ধ পর্যন্ত একাডেমিক আগ্রহের বিষয় ছিল। (হোরড্রোকার্বন জ্বালানির তুলনায় বোরাণস এবং তাদের ডেরাইভেটিভসগুলি জ্বলনের তাপ অনেক বেশি।) উইলিয়াম নুন লিপসকম, জুনিয়র, ১৯ chemical6 সালে রসায়নের জন্য নোবেল পুরস্কার পেয়েছিলেন, "বোর্নেসের কাঠামোগত কাঠামোগত সমস্যা সম্পর্কে আলোকপাতকারী গবেষণার জন্য তাঁর গবেষণার জন্য," যখন শ্লেসিংগার এর একটি of হার্বার্ট চার্লস ব্রাউন শিক্ষার্থীরা তাঁর হাইড্রোপারেশন রিঅ্যাকশন (১৯৫6) এর জন্য ১৯৯৯ সালের পুরষ্কার ভাগ করে নিয়েছিল, বিএইচের উল্লেখযোগ্যভাবে সহজ সংযোজন3 (বিএইচ 3 · এস আকারে) ঘরের তাপমাত্রায় ইথার সলভেন্টস (এস) এর মধ্যে অসম্পৃক্ত জৈব যৌগগুলিতে (অর্থাত্ অ্যালকেনস এবং অ্যালকিনেস) পরিমাণগতভাবে অর্গানবোরান উত্পাদন করতে (যা সম্পূর্ণ বা পুরোপুরি এগিয়ে যায় এমন একটি প্রতিক্রিয়া হিসাবে) সমাপ্তি)। জলবিদ্যুৎ প্রতিক্রিয়া ঘটিত জৈব সংশ্লেষের ক্ষেত্রে গবেষণার নতুন উপায় উন্মুক্ত করে।
স্টক দ্বারা প্রস্তুত করা বোরাণগুলির সাধারণ রচনা বি এন এইচ এন + 4 এবং বি এন এইচ এন + 6 ছিল তবে আরও জটিল প্রজাতি, উভয়ই নিরপেক্ষ এবং নেতিবাচক (অ্যানিয়োনিক) জানা যায়। বোরনের হাইড্রাইড কার্বন ব্যতীত অন্য যে কোনও উপাদানগুলির চেয়ে অনেক বেশি। সহজতম বিচ্ছিন্ন বোরেন হ'ল বি 2 এইচ 6, ডাইবোরেন (6)। (প্রথম বন্ধনে আরবি সংখ্যা হাইড্রোজেন পরমাণুর সংখ্যা নির্দেশ করে।) এটি সর্বাধিক বিস্তৃত অধ্যয়নকারী এবং সিনথেটিকভাবে দরকারী রাসায়নিক মধ্যস্থতাগুলির মধ্যে একটি। এটি বাণিজ্যিকভাবে উপলভ্য, এবং বহু বছর ধরে সরাসরি বা অপ্রত্যক্ষভাবে বহু বোর্ন এবং তাদের ডেরাইভেটিভগুলি এ থেকে প্রস্তুত হয়েছিল। ফ্রি বিএইচ 3 (এবং বি 3 এইচ 7) খুব অস্থির, তবে এগুলি লুইস ঘাঁটি (বৈদ্যুতিন-দাতা অণু) geg, বিএইচ 3 · এন (সিএইচ 3) 3 দিয়ে স্থিতিশীল অ্যাডিক্টস (সংযোজন পণ্য) হিসাবে পৃথক করা যায় । বোর্নসগুলি সলিড, তরল বা গ্যাস হতে পারে; সাধারণভাবে, তাদের গলে যাওয়া এবং ফুটন্ত পয়েন্টগুলি ক্রমবর্ধমান জটিলতা এবং আণবিক ওজনের সাথে বৃদ্ধি পায়।
Boranes গঠন এবং বন্ধন
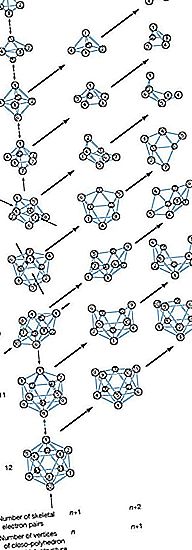
কার্বন যৌগগুলির সরল চেইন এবং রিং কনফিগারেশনগুলি প্রদর্শন করার পরিবর্তে আরও জটিল বোরানগুলিতে বোরন পরমাণুগুলি পলিহেড্রনের কোণে অবস্থিত, যা ডেলটাহেড্রন (ত্রিভুজাকার মুখযুক্ত পলিহেড্রন) বা ডেল্টহেড্রাল টুকরা হিসাবে বিবেচিত হতে পারে। এই বোরন ক্লাস্টারগুলির বোঝার বিকাশ করা রসায়নবিদদের অন্যান্য অজৈব, অর্গানমেটালিক এবং ট্রানজিশন-মেটাল ক্লাস্টার যৌগগুলির রসায়নকে যৌক্তিকরূপে গড়ে তুলতে সহায়তা করেছে।
ইন্টারন্যাশনাল ইউনিয়ন অফ পিওর অ্যান্ড অ্যাপ্লাইড কেমিস্ট্রি (আইইউপিএসি) দ্বারা প্রস্তাবিত নামকরণের বেশ কয়েকটি সিস্টেমের মধ্যে একটি বৈশিষ্ট্যযুক্ত কাঠামোগত উপসর্গ নিয়োগ করে: (১) ক্লোসো- (লাতিন ক্লোভিস থেকে "ক্লোভো" এর একটি দুর্নীতি, যার অর্থ "খাঁচা"), ডেল্টহেড্রনস এন বোরন পরমাণু; (২) নিডো- (ল্যাটিন নিডাস থেকে, যার অর্থ "নীড়"), নিরবিদ্ধ কাঠামো যেখানে বি এন ক্লাস্টার একটি (এন + 1) -র কোণযুক্ত পলিহেড্রন-এর কোণে দখল করে, যার মধ্যে একটি ক্লোসো-পলিহেড্রন একটি নিখোঁজ শীর্ষবিন্দু রয়েছে; ()) আরচনো- (গ্রীক, যার অর্থ “মাকড়সার জাল”), আরও বেশি উন্মুক্ত ক্লাস্টারগুলি বোরন পরমাণুগুলির সাথে একটি (এন + ২) -র কোণযুক্ত পলিহেড্রন — অর্থাত্, দুটি নিখোঁজ বিশিষ্ট বিশিষ্ট ক্লোসো-পলিহেড্রন রয়েছে; (৪) হাইফো- (গ্রীক, যার অর্থ "বুনন" বা "একটি নেট"), সর্বাধিক উন্মুক্ত গুচ্ছ, বোরন পরমাণুগুলির একটি (এন + 3) -র কোণযুক্ত ক্লোসো-পলিহেড্রনের কোণে দখল করেছে; এবং (5) ক্লাডো- (গ্রীক, যার অর্থ "শাখা"), এন বোরন পরমাণু দ্বারা দখল করা একটি এন + 4-ভার্টেক্স ক্লোসো-পলিহেড্রন এর n শীর্ষে অবস্থিত। হাইফো- এবং ক্লেডো-সিরিজের সদস্যগণ বর্তমানে কেবল বোরেন ডেরিভেটিভস হিসাবে পরিচিত। এই পলিহেড্রাল বুরেন গুচ্ছগুলির মধ্যে দুটি বা তার বেশি সংখ্যার মধ্যে যোগসূত্রটি উপসর্গ কঞ্জাক্টো- দ্বারা বোঝানো হয়েছে (লাতিন, যার অর্থ "একসাথে যোগদান")। উদাহরণস্বরূপ, কনজেক্টো-বি 10 এইচ 16 দুটি বি 6 এইচ 9 ইউনিটগুলিতে বি ― বি বন্ডের মাধ্যমে বি 3 এইচ 8 ইউনিটগুলিতে যোগদান করে উত্পাদিত হয় ।
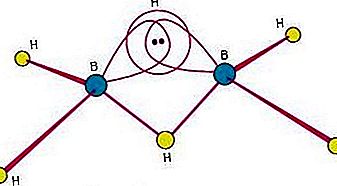
বোর্নেসের প্রতি প্রচুর আগ্রহের একটি কারণ হ'ল তারা অন্য কোনও শ্রেণীর যৌগের চেয়ে পৃথক কাঠামো রাখে। যেহেতু বোরাণগুলিতে বন্ধনে মাল্টিসেন্ট্রে বন্ধন জড়িত থাকে, যার মধ্যে তিন বা ততোধিক পরমাণু বন্ধনকারী ইলেক্ট্রনগুলির একটি জুড়ি ভাগ করে, বোরাসকে সাধারণত ইলেক্ট্রন-ঘাটতি পদার্থ বলা হয়। ডিবোরেনে (6) নিম্নলিখিত কাঠামো রয়েছে:
এই কাঠামোতে তিন-কেন্দ্রের সেতুবন্ধন জড়িত, যার মধ্যে একটি ইলেকট্রন জোড়া তিনটি (দুটি নয় বরং) পরমাণুর মধ্যে ভাগ করা হয় - দুটি বোরন পরমাণু এবং একটি হাইড্রোজেন পরমাণু। (রাসায়নিক বন্ধন দেখুন: রাসায়নিক বন্ধনের উন্নত দিক: ত্রি-কেন্দ্রিক বন্ধনের আলোচনার জন্য বোরানস।) বোরনের সাধারণ কোভলেন্ট বন্ড ছাড়াও এই ধরণের বন্ধন গঠনের ক্ষমতা জটিল পলিহেড্রাল বোরাস গঠনের দিকে পরিচালিত করে।










![ভ্যান ডাইকের থিন ম্যান চলচ্চিত্রের পরে [১৯3636] ভ্যান ডাইকের থিন ম্যান চলচ্চিত্রের পরে [১৯3636]](https://images.thetopknowledge.com/img/entertainment-pop-culture/0/after-thin-man-film-van-dyke-1936.jpg)
