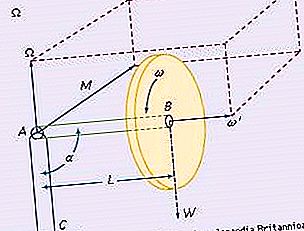
ইলাস্টিক বৈশিষ্ট্য
বিরল-পৃথিবী ধাতব অন্যান্য বৈশিষ্ট্যগুলির মতো, বিরল-পৃথিবী ধাতবগুলির স্থিতিস্থাপক মডুলি অন্যান্য ধাতব উপাদানগুলির মধ্যভাগে পড়ে। স্ক্যানডিয়াম এবং ইটরিয়ামের মানগুলি ল্যান্থানাইডের শেষ সদস্যগুলির মতো (ইরবিয়াম থেকে লুটিয়াম) সমান। ক্রমবর্ধমান পারমাণবিক সংখ্যা সহ ইলাস্টিক মডুলাসে একটি সাধারণ বৃদ্ধি রয়েছে is সেরিয়ামের জন্য অসাধারণ মানগুলি (কিছু 4f বন্ডিং), এবং ইটার্বিয়াম (দ্বিগুণ) স্পষ্ট।
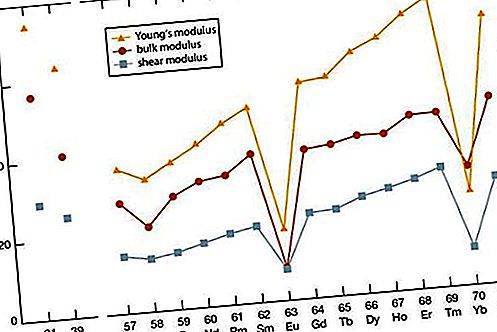
যান্ত্রিক বৈশিষ্ট্য
বিরল-পৃথিবী ধাতুগুলি দুর্বল বা বিশেষত শক্তিশালী ধাতব উপাদান নয় এবং এগুলি কিছুটা পরিমিত নমনীয়তা প্রদর্শন করে। যেহেতু যান্ত্রিক বৈশিষ্ট্যগুলি ধাতবগুলির বিশুদ্ধতা এবং তাদের তাপীয় ইতিহাসের উপর বেশ দৃ strongly়ভাবে নির্ভরশীল, তাই সাহিত্যে উল্লিখিত মানগুলির তুলনা করা কঠিন। চূড়ান্ত শক্তি প্রায় 120 থেকে 160 এমপিএ (মেগাপাসকল) এবং নমনীয়তা প্রায় 15 থেকে 35 শতাংশ পর্যন্ত পরিবর্তিত হয়। ইয়েটারবিয়ামের শক্তি (ইউরোপিয়াম পরিমাপ করা যায়নি) অনেক ছোট, 58 এমপিএ, এবং নমনীয়তা বেশি, প্রায় 45 শতাংশ, যেমন বিভাজক ধাতুর জন্য প্রত্যাশিত হবে।
রাসায়নিক বৈশিষ্ট্য
বায়ু সহ বিরল-পৃথিবী ধাতবগুলির প্রতিক্রিয়াশীলতা হালকা ল্যান্থানাইড এবং ভারী মধ্যে একটি উল্লেখযোগ্য পার্থক্য প্রদর্শন করে। ভারী ল্যান্থানাইডস (লুটিয়ামের মাধ্যমে গ্যাডোলিনিয়াম), স্ক্যান্ডিয়াম এবং ইটিরিয়ামের তুলনায় হালকা ল্যান্থানাইডগুলি আরও বেশি দ্রুত অক্সাইডাইজ করে। গঠিত অক্সাইড পণ্যটির পরিবর্তনের কারণে এই পার্থক্যটি কিছুটা অংশ। হালকা ল্যান্থানাইডস (নিউডিমিয়ামের মাধ্যমে ল্যান্থানাম) ষড়ভুজ এ-টাইপ আর 2 ও 3 কাঠামো গঠন করে; মাঝারি ল্যান্থানাইডস (গ্যাডোলিনিয়ামের মাধ্যমে সমারিয়াম) মনোক্লিনিক বি-টাইপ আর 2 ও 3 ফেজ গঠন করে; ভারী ল্যান্থানাইডস, স্ক্যান্ডিয়াম এবং ইটরিয়ামগুলি কিউবিক সি-টাইপ আর 2 ও 3 সংশোধন করে। এ-টাইপ বাতাসে জলীয় বাষ্পের সাথে বিক্রিয়া করে একটি অক্সিহাইড্রক্সাইড তৈরি করে, যার ফলে সাদা প্রলেপ পড়তে থাকে এবং তাজা ধাতব পৃষ্ঠটি প্রকাশ করে জারণকে এগিয়ে যেতে দেয়। সি-টাইপ অক্সাইড একটি শক্ত, সুসংগত আবরণ গঠন করে যা আরও জারণ রোধ করে, অ্যালুমিনিয়ামের আচরণের মতো। সামারিিয়াম এবং গ্যাডোলিনিয়াম, যা বি-টাইপ আর 2 ও 3 ফেজ গঠন করে, ভারী ল্যান্থানাইডস, স্ক্যান্ডিয়াম এবং ইটরিয়ামের তুলনায় কিছুটা দ্রুত অক্সাইডাইজ করে তবে আরও একটি জড়িত আবরণ গঠন করে যা আরও জারণ বন্ধ করে দেয়। এ কারণে, হালকা ল্যান্থানাইডগুলি অবশ্যই ভ্যাকুয়ামে বা জড় গ্যাসের পরিবেশে সংরক্ষণ করতে হবে, ভারী ল্যান্থানাইডস, স্ক্যান্ডিয়াম এবং ইটরিয়ামটি কোনও জারণ ছাড়াই কয়েক বছর ধরে খোলা বাতাসে ফেলে রাখা যেতে পারে।
ইউসোপিয়াম ধাতু, যা একটি সিসি কাঠামো রয়েছে, আর্দ্র বাতাসের সাথে বিরল পৃথিবীর যে কোনও একটির দ্রুততম জারণ করে এবং জড় গ্যাসের বায়ুমণ্ডলে সর্বদা পরিচালনা করা দরকার। ইউরোপিয়ামের বিক্রিয়া পণ্যটি যখন আর্দ্র বাতাসের সংস্পর্শে আসে তখন হাইড্রেট হাইড্রোক্সাইড, ইইউ (ওএইচ) 2 ― এইচ 2 ও, যা একটি অস্বাভাবিক প্রতিক্রিয়া পণ্য কারণ অন্য সমস্ত বিরল-পৃথিবী ধাতু একটি অক্সাইড গঠন করে।
ধাতুগুলি হাইড্রোফ্লোরিক অ্যাসিড (এইচএফ) ব্যতীত সমস্ত অ্যাসিডের সাথে জোর প্রতিক্রিয়া দেখায়, এইচ 2 গ্যাস নির্গত করে এবং এর সাথে সম্পর্কিত বিরল-পৃথিবী – আয়ন যৌগ গঠন করে। হাইড্রোফ্লিউরিক অ্যাসিডে রাখলে বিরল-পৃথিবী ধাতুগুলি একটি দ্রবীভূত আরএফ 3 লেপ তৈরি করে যা পরবর্তী কোনও প্রতিক্রিয়া প্রতিরোধ করে।
বিরল-পৃথিবী ধাতুগুলি হ'ল হাইড্রোজেন গ্যাসের সাথে সহজেই আরএইচ 2 গঠন করে এবং শক্ত হাইড্রাইডিং পরিস্থিতিতে, আরএইচ 3 ধাপ sc স্ক্যানডিয়াম ব্যতীত, যা ট্রাইহাইড্রাইড গঠন করে না।
যৌগিক
বিরল-পৃথিবী উপাদানগুলি পর্যায় সারণীতে গ্রুপ 7 টি ধাতব (ম্যাঙ্গানিজ, টেকনিটিয়াম এবং রেনিয়াম) এর ডানদিকে এবং ডানদিকে সমস্ত উপাদান সহ কয়েক হাজার সংখ্যক যৌগ তৈরি করে, আরও বেরিলিয়াম এবং ম্যাগনেসিয়াম যা খুব দূরে রয়েছে which 2 গোষ্ঠীতে বাম-হাতের পার্শ্ব 2 গুরুত্বপূর্ণ যৌগিক সিরিজ এবং অনন্য বৈশিষ্ট্য বা অস্বাভাবিক আচরণ সহ কিছু পৃথক যৌগগুলি নীচে বর্ণিত।
অক্সাইড
আজ অবধি অজৈব দুর্লভ-পৃথিবী যৌগিকদের বৃহত্তম পরিবার অক্সাইড studied সর্বাধিক সাধারণ স্টোচিওমিট্রিটি হ'ল আর 2 ও 3 রচনা, তবে, যেহেতু কয়েকটি ল্যান্থানাইড উপাদানগুলির মধ্যে 3+ ছাড়াও অন্যান্য ভ্যালেন্স রাজ্য রয়েছে, অন্য স্টোচিওমেট্রিগুলি রয়েছে instance উদাহরণস্বরূপ, সেরিয়াম অক্সাইড (সিও 2), প্রেসোডেমিয়াম অক্সাইড (PR 6 O 11)), টারবিয়াম অক্সাইড (টিবি 4 হে 7), europium অক্সাইড (EuO), ও ইইউ 3 হে 4 । বেশিরভাগ আলোচনাই বাইনারি অক্সাইডগুলিকে কেন্দ্র করবে তবে টের্নারি এবং অন্যান্য উচ্চ-আদেশ অক্সাইডগুলিও সংক্ষেপে পর্যালোচনা করা হবে।